在氧化还原反应中,失去电子的物质称为还原剂,因为它放出电子而使另一物质被还原;得到电子的物质称为氧化剂,因为它取得电子而使另一物质被氧化。还原剂具有还原性质,氧化剂具有氧化性质。氧化剂和还原剂有强弱之分,获得电子能力强的物质为强氧化剂,反之为弱氧化剂;失去电子能力强的物质为强还原剂,反之为弱还原剂。
在水质分析中常用的氧化剂有:K2Cr2O7、KMnO4、HNO3、浓H2SO4、MnO2、O2、Cl2、I2等;常用的还原剂有:Na2S2O3、Na2C2O4、FeSO4、KI、SO2、Fe等。
氧化剂氧化能力或还原剂还原能力的大小与物质的价态有关,可以用有关电对的电极电位来衡量。例如硫元素有+6(CO2-4)、+4(SO2)、0(S)、-2(H2S)四种价态,氧化能力最强的是最高价的SO2-4,还原能力最强的是最低价H2S,若一个氧化还原半反应为:
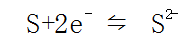
氧化态(S)得到电子变成还原态(S2-),它们构成一个氧化还原电对:S/S2-。点对中氧化态的氧化能力与还原态的还原能力的相对大小由该电对的电极电位决定。